- Strukturní vzorec - Structural formula - qwe.wiki
- Kyselina trihydrogenarsenitá - strukturní elektronový vzorec – Ontola
- Elektronový strukturní vzorec kyslíku
Stejným činidlem reaguje fenol chemicky a vytváří se trifenolát, který má fialovou barvu. Kvantitativní reakcí na rezorcinol je vzhled tmavě fialového barvení za přítomnosti chloridu železitého. Postupně barva roztoku zmizí černě. Reakční vzorec, který slouží k rozpoznání fenolu a některých jeho homologů, je FeCl 3 (chlorid železitý). Hydroxybenzen, naftol, thymol jsou všechny fenoly. Obecný vzorec a složení látek umožňuje určit, zda tyto sloučeniny patří do aromatických řad. Všechny organické látky obsahující ve svém vzorci fenylový zbytek C 6 H 5, s níž jsou hydroxylové skupiny přímo vázány, vykazují zvláštní vlastnosti. Odlišují se od alkoholů v lepší vyjádřené kyselosti. Ve srovnání s látkami homologní série benzenu jsou fenoly aktivnějšími chemickými sloučeninami.
kosterní formule
Kosterní vzorce jsou standardní zápis pro více komplexních organických molekul. V tomto typu diagramu, nejprve použitý organický chemik Friedrich August Kekulé von Stradonitz, atomy uhlíku jsou naznačeny být umístěny na vrcholech (rohů) a konce úseček, než je označen s atomovým symbol C. vodíkové atomy připojené až atomů uhlíku nejsou uvedeny: každý atom uhlíku se rozumí, že jsou spojeny s dostatkem atomy vodíku, aby atom uhlíku, čtyř vazeb. Přítomnost kladné nebo záporné náboje na atomu uhlíku, který se na místo jednoho z předpokládaných atomů vodíku. Vodíkové atomy připojené na atomy jiné než uhlík musí být explicitně. Indikace stereochemie
Existuje několik metod, aby si představit trojrozměrné uspořádání atomů v molekule ( stereochemie). Stereochemie v kosterních vzorcích
Kosterní vzorec strychnin. Pevná zaklíněný vazba vidět například na dusíku (N), v horní části označuje vazbu směřující nad-the-rovině, zatímco přerušovaná zaklínění vazba vidět například na atom vodíku (H), na dně označuje pod-the-letadlo vazbu.
• Určit typ sloučeniny • Určit středový atom • Určit počet valenčních elektronů jednotlivých atomů (Pozor: u kationtů je počet valenčních elektronů menší, u aniontů větší o počet, který odpovídá náboji! )
Kyselina trihydrogenarsenitá - strukturní elektronový vzorec – Ontola
- Neuvěřitelný Beta rozpad a Elektronový záchyt.
- Hledejte: Karla-Mráčková.wmv | Ulož.to
- Močovina – Wikipedie
- Předpis SŽDC D3 Účinnost od ppt stáhnout
- Bílý kámen 2010 qui me suit
- Výpočet cash flow vzorec
- Hry na ps4 v češtině
- Zámek červená lhota kraj
- Bastardi 3 celý film
- Hra o trůny 8 série počet dílů
- Určování slovních druhů pracovní list
- Molekulární a strukturní vzorec fenolu
Strukturní vzorec o chemické sloučeniny je grafické znázornění molekulární struktury, ukazující, jak jsou atomy uspořádány. Chemická vazba je rovněž uvedena v molekule, a to buď explicitně nebo implicitně. Na rozdíl od chemických vzorců, které mají omezený počet symbolů a jsou schopné pouze omezeného popisné síly, strukturní vzorce poskytují kompletní geometrické znázornění molekulární struktury. Například, mnoho chemických sloučenin existovat v různých izomerních formách, které mají rozdílné enantiomerní struktury, ale stejný chemický vzorec. Strukturní vzorec je schopen uvést uspořádání atomů v trojrozměrném prostoru tak, že se chemický vzorec nemusí být schopen dělat. Několik systematické chemické pojmenování formáty, jak v chemických databázích, se používají, které jsou ekvivalentní, a tak silný jako geometrické struktury. Tyto chemické názvosloví systémy zahrnují SMILES, InChI a CML. Tyto systematické chemické názvy mohou být převedeny na strukturní vzorce a naopak, ale chemici téměř vždy popisují chemické reakce nebo syntézu použitím strukturní vzorce, spíše než chemické názvy, protože strukturní vzorce umožňují chemik pro vizualizaci molekul a strukturální změny, které se vyskytují v je v průběhu chemických reakcí.
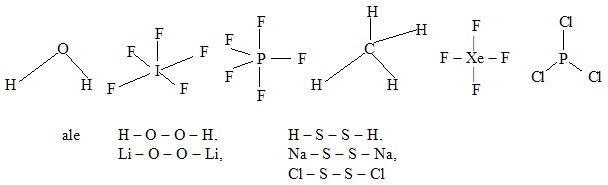
Elektronový strukturní vzorec kyslíku
Lewis struktury
Lewis struktury (nebo "dot struktury Lewis") jsou ploché grafické vzorce, které ukazují, atomovou konektivitu a volný elektronový pár nebo nepárové elektrony, ale ne trojrozměrné struktury. Tento zápis se používá hlavně pro malé molekuly. Každý řádek představuje dva elektrony s jednoduchou vazbou. Dva nebo tři paralelní linie mezi dvojicemi atomů představují dvojné nebo trojné vazby, v tomto pořadí. Alternativně, dvojice bodů může být použit k reprezentaci vazebné páry. Kromě toho jsou všechny non-vázané elektrony (spárované nebo nespárované) a jakékoliv formální poplatků jsou uvedeny na atomech. kondenzované formule
V časných publikacích organické chemie, kde je použití grafiky byl silně omezen, typografický systém vznikl popsat organické struktury v řádku textu. I když tento systém má tendenci být problematické v aplikaci na cyklických sloučenin, zůstává pohodlný způsob představují jednoduché struktury:
CH 3 CH 2 OH ( ethanol)
Závorky se používají k označení více shodných skupin, což ukazuje vazbu k nejbližšímu nevodíkovému atomu na levé straně, když se objeví v rámci obecného vzorce, nebo k atomu na pravé straně, když se objeví na začátku vzorce:
(CH 3) 2 CHOH nebo CH (CH 3) 2 OH ( 2-propanol)
Ve všech případech jsou zobrazeny všechny atomy, včetně vodíkových atomů.
2. 3 Úprava strukturních vzorců na elektronové strukturní
Úprava strukturních vzorců na elektronové strukturní probíhá tak, že do strukturních vzorců:
Doplníme násobné vazby tak, aby celkový počet vazeb vycházejících z každého atomu byl roven absolutní hodnotě oxidačního čísla tohoto atomu. Toto pravidlo neplatí v případě, že jsou na sebe v molekule vázány dva atomy téhož prvku (např. v molekule peroxidu vodíku – oxidační číslo kyslíku je –I, ale vycházejí z něj dvě vazby). V dvojatomových molekulách plynných prvků lze na násobnost vazby usuzovat na základě diagramu molekulových orbitalů (učivo obecné chemie). Zapamatujme si, že v molekule O 2 je dvojná vazba, v molekule N 2 je vazba trojná a v molekule H 2 a v molekulách halogenů jsou vazby jednoduché. Doplníme valenční elektrony tak, aby se počet valenčních elektronů ve valenční sféře každého z atomů shodoval s číslem skupiny, v níž se prvek nachází v periodickém systému prvků (např. S je v VI. podskupině, má tedy 6 valenčních elektronů, F je v VII. podskupině, má tedy
7 valenčních elektronů, B je v III.
Tomáš Svěrák, CSc. (člen)
Date of defence
2011-06-22
Process of defence
Bakalářská práce se zabývala přípravou softwaru pro výuku tvorby elektronových struktur používaných v e-learningu. Prezentace byla ilustrativní a přednesená s dostatečnou jasností. Na dotazy oponentky odpovídala správně. Result of the defence
práce byla úspěšně obhájena
Source
NOVÁKOVÁ, K. Elektronové strukturní vzorce Tvorba e-learningových studijních materiálů [online]. Brno: Vysoké učení technické v Brně. Fakulta chemická. 2011.
- Soudkyně barbara herci con
- Spolkové země rakouska sousedící s čr
- Kdo vlastní seznam cz
- Tenká červená linge de lit
- Český film 2015 cpanel